
AUTEUR :
Dr Vet. Graham ZOLLER – Dip.ECVZ
Présentation du cas
Une lapine naine, stérilisée, âgée de 1 an et 9 mois, est présentée pour une modification de l’apparence des deux yeux évoluant depuis 2 mois. Une diminution de l’activité est rapportée sans altération de l’appétit ou du transit. Habituellement, la lapine vit seule et reçoit une alimentation constituée de foin et de légumes variés. Aucun antécédent médical n’est rapporté. Le bilan biochimique et les radiographies du crâne ne révèlent aucune anomalie. Un traitement de fenbendazole et de sulfamides-triméthoprime est administré sans amélioration notable de la situation.
À l’examen clinique, la lapine présente un bon état de chair et un tempérament vif, alerte et réactif. La sensibilité et la motricité des paupières sont normales. Pour les deux yeux, l’examen ophtalmologique révèle un réflexe à l’éblouissement et des réflexes photomoteurs direct et indirect normaux, ainsi qu’une discrète hyperhémie scléro-conjonctivale associée à un globe oculaire proéminent (Fig. 1A). L’évaluation à la lampe à fente montre une augmentation de la profondeur de la chambre antérieure bilatéralement. Les cristallins sont d’apparence normale. Un fond d’œil est réalisé (Fig. 1B).
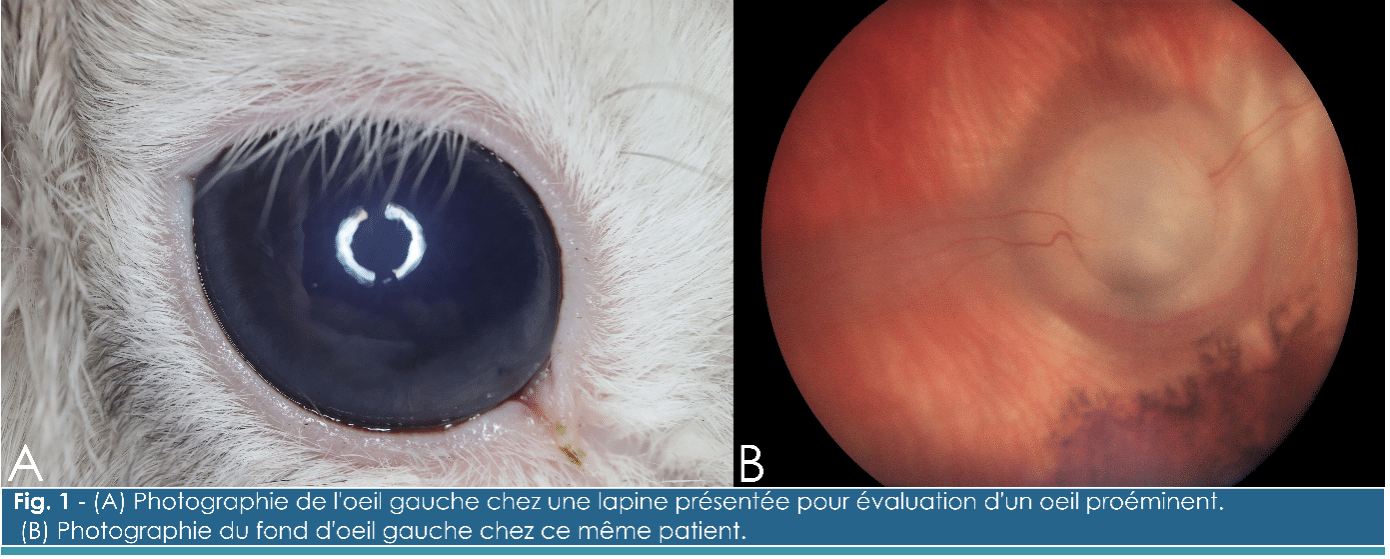
Questions
- Quel est votre diagnostic différentiel en cas de globe oculaire proéminent chez un lapin ?
- Quelles sont les particularités du fond d'œil chez le lapin ?
- A l'aide des données anamnestiques et cliniques, quel est votre diagnostic ? Quelles peuvent en être les causes ?
- Quels examens complémentaires proposeriez-vous ?
- Quelles sont les options thérapeutiques possibles ?
Réponses aux questions
1. Quel est votre diagnostic différentiel en cas de globe oculaire proéminent chez un lapin ?
Un globe oculaire proéminent chez un lapin doit inviter à envisager une proptose du globe oculaire (i.e. une protrusion du globe oculaire en dehors de l’orbite), une exophtalmie (i.e. un globe oculaire repoussé vers l’avant par un effet de masse intra-orbitaire mais demeurant dans son orbite) et une hydrophtalmie (i.e. un globe oculaire de taille augmentée demeurant dans son orbite). Ces anomalies peuvent être distinguées cliniquement :
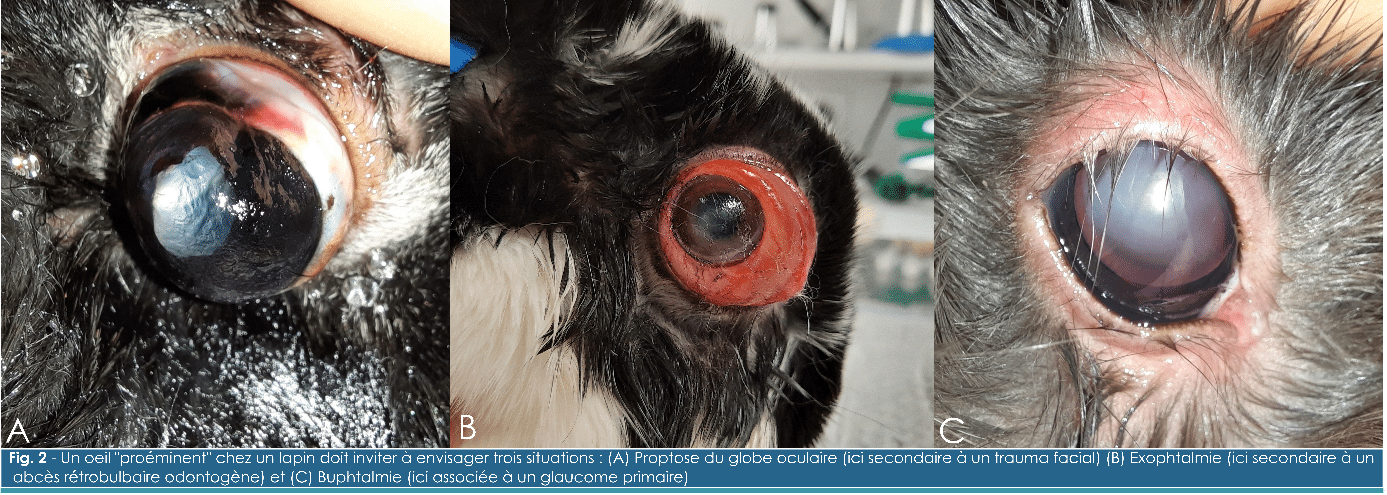
- La proptose du globe oculaire (Fig. 2A) est rare chez le lapin et fait le plus souvent suite à un trauma sévère. La proptose peut être associée à un strabisme secondaire à la déchirure des muscles extra-oculaires. Par ailleurs, des signes de trauma intra-oculaires (p.ex. hyphéma) ou de trauma maxillofaciaux peuvent être observés.
- Les exophtalmies (Fig. 2B) sont fréquentes chez le lapin. Elles peuvent être secondaires à l’existence de tumeur (p.ex. lymphome), d’abcès (p.ex. odontogène, pasteurellose), de kyste parasitaire (p.ex. cestodes), d’une adénite idiopathique, d’une cellulite rétrobulbaire ou d’une congestion du sinus veineux rétrobulbaire. Le sinus veineux rétrobulbaire est une particularité anatomique chez le lapin. Une congestion peut se produire physiologiquement (réponse de stress), lors d’anomalie vasculaire ou bien en cas de mauvais retour veineux (p.ex. masse médiastinale telle qu’un lymphome thymique ou un adénocarcinome). Lors d’exophtalmie, l’œil est repoussé vers l’avant de sorte que la conjonctive et la troisième paupière font généralement protrusion. La rétropulsion digitée du globe est généralement difficile voire impossible lors d’exophtalmie. D’autres signes cliniques peuvent être observés selon l’origine de l’exophtalmie (p.ex. malocclusion dentaire, suppurations intra-orales ou encore une lymphadénomégalie mandibulaire).
- Une hydrophtalmie (Fig. 2C) est pathognomonique d’une augmentation de la pression intra-oculaire. Une mégalocornée, un œdème cornéen et des stries de Haab peuvent être associés à une hydrophtalmie.
2. Quelles sont les particularités liées à l'examen du fond d'œil chez le lapin ?
Chez le lapin, l'évaluation du fond d'œil peut être difficile en raison de la petite taille du globe oculaire. Le fond d'œil peut être évalué par ophtalmoscopie indirecte à l'aide d'une lentille de +20 à +40 dioptries ou par ophtalmoscopie directe en réglant la roulette de dioptrie à '0'. La mydriase peut être lente voire impossible à induire pharmacologiquement dans cette espèce car les mydriatiques topiques ont une efficacité imprévisible pour deux raisons : (1) 40% des lapins produisent des atropinases ce qui limite l'utilisation d'atropine 1 et (2) les agents mydriatiques peuvent se lier aux pigments mélaniques uvéaux chez les patients ayant un iris pigmenté.2 Cela étant dit, le tropicamide est l'agent recommandé pour l'induction d'une mydriase chez le lapin. La mydriase est obtenue après un délai de 20 à 40 minutes et persiste généralement entre 4 et 8 heures après l'application de tropicamide. La vitesse d'action peut être accélérée en utilisant de la phényléphrine 10% topique de façon concomitante.
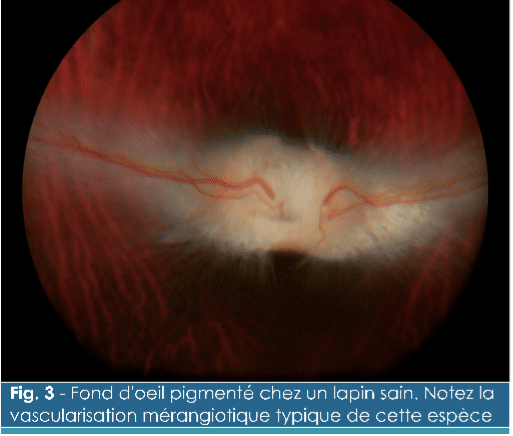
L'apparence du fond d'œil chez le lapin (Fig. 3) présente plusieurs particularités :
- Une absence de tapis clair – La rétine présente une zone horizontale contenant une forte densité de photorécepteurs que l'on appelle la bande visuelle. Cette bande permet au lapin de visualiser tout l'horizon à tout instant. Les bâtonnets sont les photorécepteurs les plus nombreux et confèrent au lapin une bonne vision nocturne malgré l'absence de tapetum lucidum. Le fond d'œil est rose ou brun selon la pigmentation et les vaisseaux choroïdiens peuvent être observés chez la plupart des patients.
- Une vascularisation rétinienne de type mérangiotique – Les vaisseaux sanguins de la rétine suivent les ramifications nerveuses myélinisées du nerf optique. Ainsi, ils se ramifient latéralement (temporalement) et médialement (nasalement) à partir de la papille optique en suivant une ligne horizontale parallèle et dorsale à la bande visuelle. De ce fait, aucune structure vasculo-nerveuse n'est superposée à la bande visuelle, ce qui améliore la sensibilité visuelle mais engendre une grande zone horizontale aveugle dans la partie ventrale du champ de vision.3
- La papille optique est dorsale, large, profonde et possède une dépression centrale physiologique – La sclère est dépourvue de lame criblée chez le lapin. De ce fait, le nerf optique (par ailleurs très myélinisé) pénètre par une dépression sclérale située au-dessus de la ligne horizontale médiane de l'œil. Cliniquement, il faut donc regarder « vers le haut » – et non pas dans l'axe – pour observer la papille optique. Cette particularité peut rendre difficile la différenciation entre une dépression normale et une excavation de la papille du nerf optique en cas de glaucome.
3. À l'aide des données anamnestiques et cliniques, quel est votre hypothèse diagnostique et quelles peuvent en être les causes ?
Dans le cas présenté, le lapin présente un œil proéminent et qui demeure dans son orbite. L'examen clinique révèle une mégalocornée, une mydriase partielle et un œdème cornéen stromal et diffus sans protrusion de la troisième paupière. Par ailleurs, l'examen du fond d'œil révèle une excavation majeure du disque optique ainsi qu'une diminution du calibre vasculaire. Ces éléments sont prioritairement compatibles avec un glaucome.
Le glaucome est une neuropathie optique correspondant à la mort progressive des cellules ganglionnaires et de leurs axones au niveau de la rétine. Chez les animaux elle se caractérise systématiquement par une élévation de la pression intraoculaire (PIO) secondaire à la diminution de l'écoulement de l'humeur aqueuse au travers du réseau trabéculaire. Cette situation peut être liée à une anomalie primaire des voies de drainage ou bien être secondaire à l'existence d'une autre maladie intra-oculaire :
- Dans les glaucomes primaires, l'élévation de la PIO se développe en l'absence de maladies oculaires concomitantes et a une probabilité importante de développement bilatéral. Ils sont bien décrits chez les lapins néo-zélandais, chez qui une maladie génétique a été décrite, mais peuvent être observés chez toutes les espèces.4 Chez les lapins néo-zélandais, le gène incriminé (bu) est autosomal, récessif et semi-létal.5 Chez ces patients, l'angle irido-cornéen présente une dysgénésie à l'origine d'une altération du drainage de l'humeur aqueuse. L'augmentation de la pression intra-oculaire est à l'origine d'une augmentation de la taille du globe oculaire généralement observée chez les lapins âgés de 3 à 6 mois.
- Dans les glaucomes secondaires, l'augmentation de la PIO est associée à une maladie oculaire antérieure ou concomitante qui obstrue physiquement les voies d'écoulement de l'humeur aqueuse. Les glaucomes sont le plus souvent secondaires chez le lapin de compagnie (63% des cas) et sont diagnostiqués chez des patients âgés de 8 mois à 12 ans (médiane de 8 ans). Ils sont le plus souvent associés au développement d'une cataracte ou d'une uvéite dont certaines secondaires à une infection par E. cuniculi. Bien que moins fréquent, un hyphéma, une luxation du cristallin ou une masse intra-oculaire peuvent également être à l'origine d'une obstruction des voies de drainage.
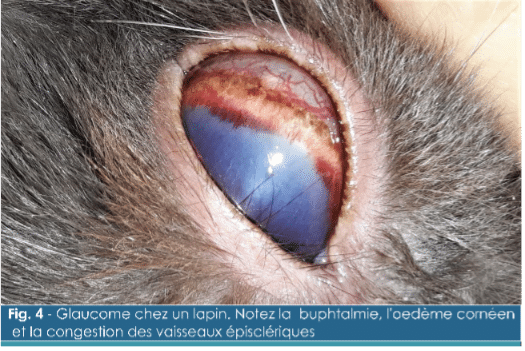
Les signes cliniques de glaucome généralement rapportés chez le lapin incluent un épiphora, et des modifications oculaires uni- ou bilatérales principalement caractérisées par une buphtalmie, une dilatation de la pupille et une cécité. La luxation du cristallin secondaire à l'augmentation de la taille du globe est une complication commune qui peut être rencontrée chez des patients conservant la vision. Une excavation de la papille optique avec dégénérescence rétinienne est une autre complication commune, qui est le plus souvent associée à de la cécité. En revanche, un œdème cornéen, des ulcères cornéens secondaire à l'œdème chronique de la cornée, des stries de Haab (brèches linéaires dans la membrane de Descemet) et une congestion vasculaire épisclérale (Fig. 4) sont moins fréquents que chez le chien. Enfin, les signes de douleur peuvent être plus difficiles à remarquer chez les lapins que chez les carnivores domestiques.
4. Quels examens complémentaires proposeriez-vous ?
Comme pour les autres espèces, l'hypothèse de glaucome doit être confirmée par une mesure de la pression intra-oculaire. Deux techniques de tonométrie ont été validées chez le lapin et des valeurs de références ont été publiées pour chacune d'entre elles (cf. Tableau 1) :
- La tonométrie par applanation (Tonopen®) nécessite l'utilisation d'une anesthésie locale (p.ex. proxymétacaïne ou tétracaïne). Chez les petits patients, un risque de toxicité systémique est possible suite à l'application d'anesthésique topique.
- La tonométrie rebond (Tonovet®) représente une alternative intéressante à la tonométrie par applanation car (1) la surface de contact avec la cornée est beaucoup plus petite et (2) le recours à une anesthésie locale n'est pas nécessaire.

Dans notre cas, la tonométrie à rebond révèle une pression intra-oculaire de 39 mm Hg. Chez le lapin de plus d’un mois, une mesure supérieure à 25 mm Hg est fortement évocatrice d’un glaucome.
La gonioscopie est un examen utile en cas de glaucome. Elle permet d’évaluer l’état de l’angle irido-cornéen et de la fente ciliaire (ouverte, étroite, fermée) ainsi que l’existence d’une maladie infiltrative de l’angle ou encore d’une uvéite antérieure occulte. La gonioscopie est aisément réalisée chez le lapin mais sera limitée en cas d’opacification cornéenne. Dans notre cas, l’œdème cornéen ne permet pas une visualisation de l’angle irido-cornéen. Une échographie de l’angle irido-cornéen pourrait être réalisée avec une sonde de 50 mmHz (Ultrasound Bio-Microscopy).
5. Quelles sont les options thérapeutiques possibles ?
L'objectif thérapeutique en cas de glaucome est de réduire la pression intra-oculaire en dessous de 20 mm Hg pour maintenir ou restaurer la vision et diminuer la douleur associée à l'hypertension intra-oculaire.
En cas de crise aigüe, une diminution rapide de la pression intra-oculaire est recherchée. Pour cela, le traitement repose sur une diminution de l'hydratation du globe oculaire à l'aide de diurétique osmotique (p.ex. mannitol 1-2 g/kg IV sur 20 minutes qui permet de réduire la pression intra-oculaire en 1 à 2 heures pour une durée de 8 à 10 heures) et/ou une diminution de la synthèse d'humeur aqueuse à l'aide d'inhibiteur de l'anhydrase carbonique par voie injectable (p.ex. acétazolamide).
Le plus souvent, les glaucomes évoluent de façon chronique chez le lapin et le traitement repose essentiellement sur l'administration de collyres similaires à ceux utilisés en médecine canine. Ces collyres permettent :
- Une diminution de la synthèse d'humeur aqueuse à l'aide de β-bloquants (p.ex. timolol 0.5% ou betaxolol 0.5% q8-12h) et/ou d'inhibiteurs de l'anhydrase carbonique (p.ex. dorzolamide 2% ou brinzolamide 1% q8-12h). Le timolol et le dorzolamide sont tous les deux bien tolérés chez le lapin et efficaces pour la gestion à court-terme de la PIO. De plus, ils ont un effet synergique de sorte que l'utilisation d'associations (p.ex. Dualkopt® q8h) est particulièrement intéressante.
- Une augmentation de l'élimination de l'humeur aqueuse à l'aide d'agonistes des prostaglandines (p.ex. latanoprost 0,005 % q12h) ou de parasympathomimétiques myotiques (p.ex. pilocarpine)
Les traitements médicaux permettent de réduire la PIO sous 2 à 4 semaines chez 70% des lapins et de contrôler la maladie parfois jusqu'à plusieurs années. Le glaucome est une maladie évolutive et un contrôle régulier de la pression intra-oculaire est recommandé. Une attention particulière devrait être portée au développement d'effets secondaires suite à l'utilisation de ces molécules (p.ex. bradycardie, déséquilibres électrolytiques, iléus digestif). En effet, les lapins ont un globe oculaire et un volume sanguin plus petits que les chiens, de sorte que le risque d'apparition d'effets secondaires systémiques suite à l'application d'une goutte de collyre est considéré plus élevé. En cas d'effets secondaires, une diminution de la taille des gouttes instillées peut être considérée.
Une approche interventionnelle peut être considérée lorsque les traitements topiques sont inefficaces pour maintenir la pression intra-oculaire sous le seuil des 20 mm Hg (environ 30% des cas) et que la douleur n'est pas contrôlée. Dans cette situation, plusieurs options thérapeutiques peuvent être considérées :
- La destruction d'une partie du corps ciliaire (p.ex. par cyclophotocoagulation ou cycloablation) peut être considérée pour réduire la production d'humeur aqueuse.
- Un gonio-implant (valve dans la chambre antérieure) peut être mis en place pour permettre à l'humeur aqueuse d'être évacuée hors de la chambre antérieure.
- L'énucléation est indiquée lorsque l'œil n'est plus visuel et que la douleur n'est pas contrôlée.4 Une attention particulière sera portée au cours de la dissection pour éviter de perforer le sinus veineux rétrobulbaire. Une énucléation bilatérale peut être nécessaire et semble bien tolérée chez le lapin. Alternativement, une injection de gentamicine dans le corps vitré peut être utilisée pour diminuer la pression intra-oculaire
En l'absence de traitement, une atrophie des corps ciliaires peut se produire sous l'effet de la pression et induire un retour à la normale de la pression intra-oculaire.


